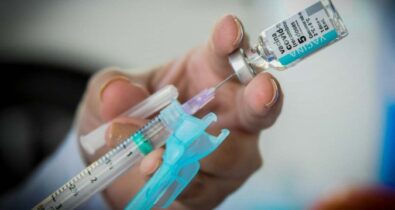
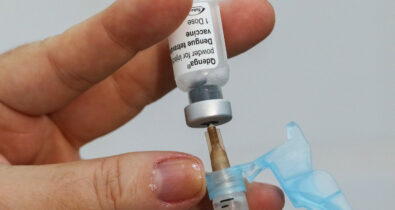
Institutos começam a estudar terceira dose para melhorar a eficácia da vacina
O estudo sobre a terceira dose contará com a participação de até 144 voluntários em duas coortes de idade: 18 a 55 anos e de 65 a 85 anos
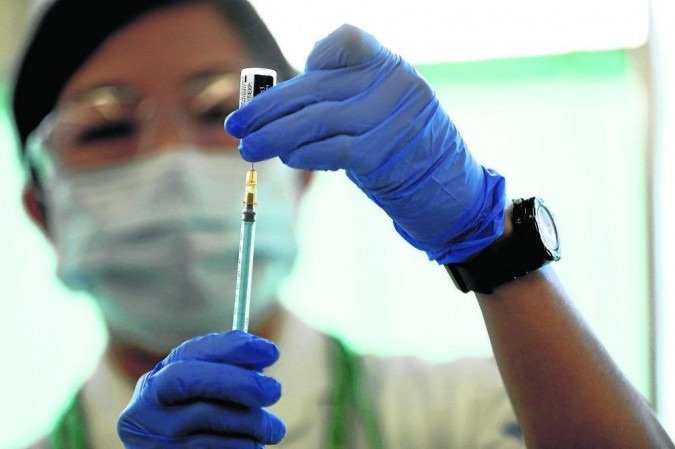
Reprodução
Para tentar combater as atuais e potenciais futuras variantes do Sars-CoV-2, a Pfizer e a BioNTech informaram, ontem, que deram início a um estudo clínico de fase 1 em que adicionaram uma terceira dose da vacina de seis a 12 meses após os participantes receberem as duas primeiras. Nessa etapa, serão avaliadas a segurança e a imunogenicidade do regime triplo: ou seja, se ele será bem tolerado pelo organismo e capaz de induzir a produção de anticorpos. O anúncio foi feito no mesmo dia em que o mundo ultrapassou o número de 2,5 milhões de mortes pela covid-19, segundo balanço da agência France-Presse (AFP) de notícias.
Em um comunicado a investidores, as duas empresas, que desenvolveram juntas uma vacina de mRNA para a covid-19, também anunciaram que buscam autorização das agências regulatórias dos EUA, a FDA, e da Europa, a Agência de Medicamentos Europeia, para um ensaio clínico de uma vacina específica para a cepa sul-africana. A linhagem B.1.351 do vírus, identificada, pela primeira vez, no país da África, já circula em boa parte do mundo e tem se mostrado mais resistente aos imunizantes disponíveis. Embora todos, até agora, tenham conseguido neutralizar o Sars-CoV-2, a eficácia é mais baixa, quando consideradas as outras cepas.
De acordo com os dois laboratórios, a ideia é fazer uma pequena alteração que permitirá “atualizar a vacina rapidamente se surgir a necessidade de proteção contra a covid-19” devido ao aparecimento de novas cepas. As empresas afirmaram que esperam buscar a validação de futuras vacinas de mRNA modificadas com uma via regulatória semelhante à que está em vigor para os imunizantes contra a gripe, que são alterados ano a ano, sem a necessidade de se realizar novos estudos.
“Embora não tenhamos visto nenhuma evidência de que as variantes circulantes resultem na perda de proteção fornecida por nossa vacina, estamos realizando várias etapas para agir de forma decisiva e estar prontos caso uma cepa se torne resistente à proteção conferida. Esse estudo de reforço é fundamental para entendermos a segurança de uma terceira dose e a imunidade contra cepas circulantes”, disse Albert Bourla, presidente do conselho e diretor executivo da Pfizer.
94% de eficácia
A vacina da Pfizer e da BioNTech tem eficácia de 94% no mundo real, segundo um estudo divulgado na quarta-feira. A pesquisa foi realizada em Israel, onde 50% da população já foi imunizada. Como a cepa sul-africana não circulava no país no momento do estudo, não é possível dizer se a substância também foi efetiva contra essa versão. Porém, no fim de janeiro, as duas companhias informaram que, em testes in vitro, o imunizante produziu anticorpos capazes de neutralizá-la.
A grande preocupação com a variante sul-africana é que, até agora, os estudos indicaram que pessoas que já foram infectadas com a cepa original têm maior probabilidade de serem contaminadas novamente. A outra desenvolvedora de uma vacina de mRNA para a covid-19, a Moderna, afirmou, na quarta-feira, que os Institutos Nacionais de Saúde dos EUA já receberam a versão atualizada para combater a cepa da África, o que permite o início dos testes.
“Nossa estratégia de desenvolvimento clínico proativo visa criar, hoje, a base que nos permitirá enfrentar os desafios de amanhã. Queremos estar preparados para diferentes cenários”, afirmou Ugur Sahin, CEO e cofundador da BioNTech. “Portanto, avaliamos um segundo reforço no regime atual, e estamos nos preparando para uma adaptação rápida da vacina para lidar com novas variantes que podem escapar da versão atual. A flexibilidade de nossa plataforma nos permite desenvolver tecnicamente imunizantes de reforço em semanas, se necessário.”
Idade variada
O estudo sobre a terceira dose contará com a participação de até 144 voluntários em duas coortes de idade: 18 a 55 anos e de 65 a 85 anos. O ensaio clínico incluirá participantes que receberam as duas doses no estudo de fase 1, de seis a 12 meses antes. Assim, será possível avaliar a segurança e a tolerabilidade de uma terceira dose independentemente do nível de títulos de anticorpos do voluntário.
Os participantes serão avaliados no momento em que receberem a terceira dose, uma semana e um mês depois. A Pfizer e a BioNTech planejam estudar a capacidade do soro desses participantes em neutralizar as cepas de Sars-CoV-2. Os participantes continuarão sendo acompanhados no estudo por até dois anos, conforme planejado originalmente.
Metade em cinco países
Até as 17h30 de ontem, foram registradas 2.500.172 mortes, 112.618.488 casos. A Europa, com 842.894 mortos, é a região mais enlutada, à frente de América Latina/Caribe (667.972) e EUA/Canadá (528.039). Cinco países (Estados Unidos, Brasil, México, Índia e Reino Unido) respondem por quase metade dos óbitos.
OMS: prioridade para covid de longa duração
A covid de longa duração — quando os sintomas se estendem por meses depois de o paciente estar livre do vírus — deve ser “uma prioridade clara” para todas as autoridades sanitárias do mundo, afirmou o escritório europeu da Organização Mundial da Saúde (OMS). “É uma prioridade clara para a OMS e da mais alta importância. Deve ser também para todas as autoridades sanitárias”, frisou o diretor para Europa da agência da ONU, Hans Kluge. Segundo Kluge, os sintomas de longa duração enfrentam com frequência “a incredulidade ou uma falta de compreensão”. As pessoas que sofrem com esse problema “devem ser ouvidas, se queremos entender as consequências a longo prazo e a cura da covid-19”, destacou. Alguns estudos começam a jogar uma luz sobre a questão, mas ainda não foi possível compreender o que leva alguns infectados a prosseguir durante meses com sintomas, como cansaço extremo, dificuldades respiratórias e problemas neurológicos e cardíacos.
Vacina da Johnson & Johnson é eficaz contra novas cepas
Administrada em apenas uma dose, a vacina desenvolvida pelo grupo Johnson & Johnson é eficaz contra duas novas variantes do causador da covid-19 — a sul-africana e a brasileira — e evita significativamente os quadros graves da doença. A taxa protetiva chega a 85%, segundo documento divulgado pela Agência de Regulação de Alimentos e Medicamentos dos Estados Unidos (FDA, em inglês). Também ontem, o grupo Pfizer/BioNTech publicou o estudo mais amplo sobre os impactos da fórmula que desenvolveram em parceria: 94% dos imunizados não desenvolveram a doença, conforme observação, “no mundo real”, de vacinados em Israel.
O órgão regulador americano analisou dados de estudos clínicos com a fórmula da Johnson & Johnson conduzidos em um grupo de 44 mil pessoas nos Estados Unidos, na África do Sul e em alguns países da América Latina, incluindo o Brasil. A pesquisa é, no momento, a em estágio mais avançado dos testes com o uso de dose única de um imunizante contra o Sars-CoV-2. Somam-se às vantagens da fórmula americana o não registro de reações alérgicas graves durante os ensaios clínicos e a facilidade de armazenamento — pode ser feito em geladeiras tradicionais.
Na análise dos dados gerais, o imunizante mostra-se 85,4% eficaz contra as formas graves da covid-19, mas a proteção cai para 66,1% em relação às manifestações mais moderadas da infecção. Considerando os dados locais, a eficácia em casos graves é de 85,9% nos EUA, 81,7% na África do Sul e 87,6% no Brasil, por exemplo. Segundo a FDA, a proteção foi considerada 14 dias depois da vacinação.
Os testes também revelaram que não foram registradas mortes em decorrência da covid-19 entre aqueles que receberam o imunizante. “Os dados apoiam a existência de um perfil de segurança favorável, sem preocupações específicas que possam impedir que uma autorização de uso emergencial seja emitida”, informou a agência estadunidense, em um comunicado.
O imunizante americano de dose única também é 100% eficaz contra a hospitalização 28 dias após ser aplicado. A taxa de 14 dias é de 85%. Não foram detectadas diferenças de eficácia em relação a idade, sexo ou raça dos participantes, incluindo pessoas mais velhas. No grupo de voluntários, 34% (14.672) tinham mais de 60 anos, um número considerado alto por especialistas. A expectativa é de que o FDA decida, ainda nesta semana, se a fórmula receberá um registro de emergência para uso no país.
Vetor viral
A vacina utiliza uma estratégia explorada em outros imunizantes para gerar proteção contra a covid-19: o uso de um vetor viral enfraquecido. No caso do fármaco americano, os desenvolvedores escolheram um adenovírus da gripe comum, que carrega uma proteína-chave do Sars-CoV-2. Ao entrar em contato com o organismo humano, ela desperta a produção de anticorpos protetores.
Juarez Cunha, presidente da Sociedade Brasileira de Imunizações (SBIm), avalia que os dados da vacina estadunidense são animadores. “É uma ótima notícia também pela alta eficácia observada na prevenção de casos graves, porque isso já desafoga o sistema de saúde, que é o nosso principal objetivo. Outro ponto a se comemorar é o fato de esse imunizante ser aplicado apenas em uma dose. É muito mais fácil imunizar toda a população dessa forma, nos poupará muito tempo”, justifica. “É interessante destacar ainda que essa empresa realiza testes com duas doses da mesma fórmula justamente para ter análises mais consistentes do seu efeito protetivo”, completa.
Para o imunologista, outro ponto que merece destaque é a eficácia do imunizante em regiões distintas, demonstrando, assim, a sua eficácia para diferentes cepas. A inclusão de um grande número de pessoas idosas nas análises é outro destaque, avalia Juarez Cunha. “Temos uma alta diversidade de analisados, de regiões diferentes que estão expostas a variantes distintas, e também uma quantidade considerável de indivíduos idosos. É muito bom observar que o efeito protetor nesse grupo que é mais suscetível ao vírus também foi alto, isso gera uma maior confiança.”